In seguito a ripetute segnalazioni in letteratura, a partire dalla seconda metà dell’anno 2003, ed ad una revisione dell’Office of Drug Safety dell’ FDA alla fine dell’anno 2004, è ormai accertata la possibilità dell’insorgenza di osteonecrosi delle ossa mascellari ( necrosi ossea avascolare mascellare) in pazienti sottoposti a chirurgia odontoiatrica che hanno utilizzato nei mesi o negli anni precedenti bifosfonati sia per via iniettiva che per os.
I bifosfonati più comunemente responsabili di tale patologia sono:
- Zolendronato/ac. Zolendroico (zometa)
- Pamidronato (aredia)
- Alendronato (fosamax)
- Risendronato (actonel)
- Clodronato (clasteon)
Questi farmaci agiscono selettivamente sul tessuto osseo, perché inibiscono la funzione degli osteoclasti e sono somministrati in tutte quelle malattie dove c’è un’aumentato riassorbimento osseo: Le principali indicazioni all’utilizzo di bifosfonati sono:
- le neoplasie maligne, frequentemente associate alle metastasi ossee (mieloma multiplo, cancro della mammella, carcinoma prostatico)
- le osteoporosi di varia natura
- la chirurgia ortopedica per stabilizzare i mezzi di osteosintesi
- le terapie croniche con corticosteroidi
- la malattia di Paget
- gli iperparatiroidismi primitivi o secondari
I bifosfonati, più specificamente, agiscono inibendo la funzione degli osteoclasti, impedendone la migrazione, ne attivano l’apoptosi e ne diminuiscono l’emivita, pertanto riducono la loro attività di rimodellamento sull’interfaccia del tessuto mineralizzato.
E’ probabile che tali molecole, impedendo il fisiologico turn-over osseo con conseguenti microdanni strutturali, ne compromettano la vascolarizzazione riducendo i livelli dei fattori di crescita per le cellule endoteliali ed inibendo, quindi, la funzione di tali cellule e l’angiogenesi.
Sono, inoltre, farmaci che non essendo metabolizzati, mantengono alte concentrazioni a livello dell’osso per un lungo periodo di tempo. Non esistono dati in letteratura sulla durata della permanenza dei bifosfonati nel tessuto osseo, sugli effetti ischemici in rapporto alla posologia, se questi siano di natura cumulativa e se dipendano dalla durata del trattamento con bifosfonati.
Aspetti clinici
Si presentano spesso come focolai osteomielitici singoli o multipli, in sede mascellare o mandibolare ed insorgono frequentemente dopo un’estrazione dentaria o altra chirurgia odontoiatrica, anche se sono stati segnalati casi sporadici senza alcuna causa apparente.
Inizialmente appaiono come banali patologie infiammatorie alveolari ma sono refrattarie alle terapie sistemiche (antibiotici per via parenterale e orale) ed alle terapie antisettiche topiche e tendono progressivamente ad estendersi alle zone limitrofe.
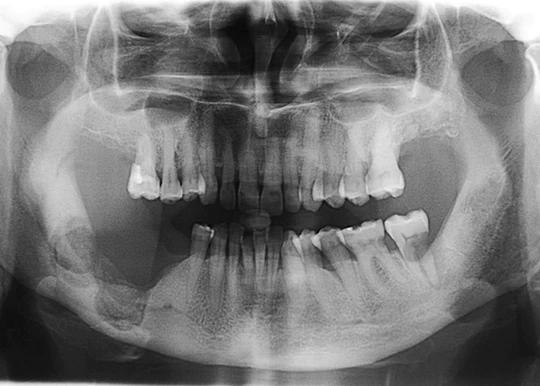
Generalmente, i pazienti, in fase avanzata, mostrano un’esposizione a livello del cavo orale di tessuto osseo necrotico accompagnata da flogosi acuta o sub-acuta in atto che tende a migliorare in seguito a terapia medica per poi rapidamente recidivare. Le indagini strumentali (ortopantomografia, TC, RMN) mostrano una zona di rimaneggiamento osseo spesso di difficile interpretazione accompagnata in maniera quasi costante da una importante reazione periostale.
Oggettiva la difficoltà di valutazione tridimensionale del segmento osseo interessato. Il quadro clinico, modulato ovviamente dalla malattia sistemica del paziente, può essere completato dalla presenza di fistole a carico dei tessuti molli e da decadimento delle condizioni generali.
La terapia della osteonecrosi da bifosfonati consiste nella somministrazione di antibiotici sistemici a cicli, guidata o meno da indagini microbiologiche, irrigazioni locali di antisettici, associata a terapia antalgica. La chirurgia viene riservata ai pazienti sintomatici che non rispondono a terapia medica e viene considerata gravata da complicanze e recidive che rendono incerta la prognosi e riducono in maniera significativa la qualità di vita del paziente.
Gli odontostomatologi, alla luce delle attuali conoscenze, dovrebbero astenersi dal praticare terapie chirurgiche in pazienti trattati con bifosfonati. La prevenzione di tale grave complicanza sembra essere, attualmente, l’unica strada percorribile, in attesa di studi a lungo termine in campo clinico e maggiormente approfonditi in campo biologico che ci forniscano ulteriori informazioni.
Nel seguente magistrale lavoro eseguito dal Dr.Crescentini, si denota una possibilità terapeutica non invasiva e dai risultati molto interessanti
Microchirugia Orale laser-magneto-assistita: un passo verso la medicina rigenerativa fisica e biotecnologica
dell’osteonecrosi avascolare infetta da difosfonati.
Crescentini F
Reparto di Odontoiatria- Div. di Microchirurgia laser-magneto assistita
Cristo Re Hospital – Rome –
Parole chiave: Bronj, osteonecrosi da difosfonato, chirurgia microscopica, laser LBO 532nm, campi magnetici, bCGF, chirurgia delle osteonecrosi mascellari e mandibolari.
Abstract
L’uso di mezzi fisici come i laser ad ottica non lineare LBO 532 nm e i Campi Elettro Magnetici Complessi (CME) ultradeboli e mezzi biotecnologici, come il concentrato di fattori di crescita bCGF (1) ottenuto da una separazione di fase del sangue è in uso nella chirurgia rigenerativa con il nome di Protocollo Chirurgico Multi Fattoriale(2).
Gli autori hanno allargato queste metodiche anche alla terapia delle osteonecrosi dei mascellari associate all’uso dei bifosfonati (3).
I metodi prevedono l’applicazione dei protocolli di decontaminazione, microfotoablazione e induzione laser-magnetica dei processi riparativi (fotoriparazione), su scaffold fibrinico, sfruttantando come supporto, solo materiale autologo e chiamando in causa l’effetto osteomorfogenetico comunemente ottenuto con questi protocolli. I casi clinici
presentati evidenziano la qualità e le modalità di riparazione con effetto osteomorfogenetico 3D e danno spunto alla comunità scientifica ad incrementare le conoscenze biologiche e biofisiche, auspicando che studi futuri possano allargare ulteriormente gli orizzonti di questo sapere affascinante che riguarda la biofisica informazionale (4) e la medicina molecolare.
Introduzione
L’osteonecrosi dei mascellari da bifosfonati è una necrosi avascolare conseguente alla farmacodinamica del pirofosfato inorganico. Questo farmaco prodotto per le sue capacità di limitare la neoangiogenesi molto utile nella patologia tumorale
ha trovato anche campo di applicazione in molte altre patologie soprattutto in quelle date da alterato metabolismo del calcio. La molecola proprio per la sua capacità a simulare l’ATP è fortemente appetibile dagli osteoclasti che, una volta inglobata, vanno in apoptosi interrompendo così il delicato e complesso meccanismo di signaling che governa le isole riparative presenti in tutte le aree scheletriche in fase di rimaneggiamento. L’osso nel suo complesso si viene così a trovare in una situazione di svantaggio nel controbilanciare tutto ciò che può alterare gli equilibri interni fra sintesi e rimodellazione.
I mascellari rappresentano le aree scheletriche che più sono sottoposte ad insulti infiammatori, infettivi e traumatici e in quanto tali sono maggiormente esposti ai fenomeni osteonecrotici che si manifestano in maniera elettiva là dove il trauma osseo si associa facilmente ad una contaminazione immediata, progressiva ed inarrestabile poiché la bocca è una fonte continua di infezioni e dal punto di vista biologico ha temperatura costante, umidità costante e residui organici.
I sintomi delle osteonecrosi hanno una stadiazione legata alla quantità del coinvolgimento tessutale in cui da piccole esposizioni si può arrivare ad ampie aree di scopertura ossea, maleodoranti, con febbre e ascessi; l’estensione grave riguarda l’apertura di fistole esterne molto ampie con coinvolgimento di strutture algogene e quindi forti episodi di dolore associati a malessere generale ed astenia. Si capisce ovviamente che anche la vita di relazione del paziente viene sconvolta.
La terapia chirurgica convenzionale, prevede la rimozione di ampie aree di osso necrotico (a volte con esiti mutilanti) e copertura immediata con lembi mucosi per prima intenzione; il must di questa terapia è quella di tenere chiuse le porte al passaggio ai microbi e una terapia antibiotica e antifungina consistente e di lunga durata.
La chirurgia microscopica permette di migliorare sensibilmente la qualità dell’intervento in relazione ad una visione magnificata dal microscopio operatorio permettendo la visione dettagliata anche delle cavità come nelle cisti e un debridment con risparmio di osso nelle lesioni osteonecrotiche.
Lo stereomicroscopio è un sistema d’ingrandimento che ci permette di curare i particolari microscopici utili in tutte le fasi della chirurgia. È costituito da un corpo centrale che contiene le lenti in sequenza alternata sia concave che convesse la cui disposizione , su due canali ( uno per la visione dell’occhio di destra ed uno per quello di sinistra) è legata alla progettazione della casa costruttrice. L’obbiettivo sta in basso verso il paziente e stabilisce oltre al primo ingrandimento anche la focale, cioè la distanza tra il microscopio e il sito da operare ( la focale varia da 200 mm a 600 mm). La visione binoculare procede verso il portaoculari che deve essere inclinabile ( da 30° a 260°) e contiene il sistema di regolazione della distanza bipupillare; gli oculari intercambiabili permettono un ulteriore ingrandimento e la regolazione delle diottrie per la messa a fuoco a seconda delle esigenze dell’operatore. Tra il corpo e il portaoculari è collocato il partitore ottico che permette i collegamenti con una telecamera e quindi la documentazione video. Per la chirurgia vale comunque il detto : “ DOVE NON E’ POSSIBILE VEDERE SI PUO’ SOLO INVENTARE” e infatti il binomio “ Sicurezza e Precisione “ è legato alla visione magnificata.
Dal punto di vista clinico come prima cosa, è essenziale intervenire sul biofilm batterico sfruttando l’effetto laser-magnetico. Il biofilm è un sistema organizzato che evolve progressivamente, in cui la dinamica della popolazione microbica assume alti livelli di complessità intrisa in una sostanza polimerica extracellulare. Sono presenti batteri ( da 2 a 15 ceppi diversi) cocchi, bacilli fuso-spirillari compresi selenomonas e tre tipi diversi di treponemi; anche i funghi di tipo candida sono presenti in coaggregazione nei diversi strati di biofilm. La matrice polimerica anionica che completa il sistema cattura minerali e nutrienti dall’ambiente e permette un alto livello comunicazionale cellula-cellula grazie ad un incremento del quorum sensing batterico. Il quorum sensing (5) è un sistema di regolazione trascrizionale dipendente dalla densità cellulare, ovvero un meccanismo che molte cellule batteriche della stessa specie utilizzano per comunicare tra di loro e per comunicare con specie diverse, comunicazione specie-specifica e inter-specie. Meccanismi di quorum sensing sono stati individuati nella quasi totalità dei batteri sia gram-negativi che gram- positivi.
Il sistema è composto da due elementi: la molecola segnale (solitamente un omoserina lattone acilato, specifico per ogni specie) e l’attivatore trascrizionale. La molecola segnale è un induttore che diffonde all’esterno della cellula originaria, e può così entrare nel citoplasma di altre cellule adiacenti. Se la concentrazione di molecola segnale all’interno di cellule della popolazione batterica è alta, questa molecola si legherà all’attivatore trascrizionale, che a sua volta attiverà o reprimerà una serie di geni, determinando l’attivazione o lo spegnimento di vie metaboliche o processi cellulari specifici.
Il laser non lineare LBO 532nm, ampiamente sperimentato per gli effetti antimicrobici di interferenza sul sistema comunicazionale e attraverso il meccanismo di optoporazione permanente (6) della membrana microbica, che innesca uno shock osmotico il quale fa esplodere la cellula batterica. Si associa inoltre l’effetto simil- ciclotronico (7) dei campi magnetici, che imprimendo un moto rotazionale ai batteri in un campo magnetico radiale complesso in relazione ed in proporzione alle cariche elettriche di superficie della membrana batterica, non permette la formazione di colonie.
Materiali e metodi
Il nostro protocollo (3) prevede una revisione delle procedure chirurgiche descritte in letteratura perché l’uso di mezzi fisici e biotecnologici introduce un nuovo punto di vista sui processi di guarigione e dove possibile, di rigenerazione, in quanto si agisce a più livelli nei meccanismi riparativi e di controllo dell’infezione

Il protocollo chirurgico prevede un assunto inderogabile: utilizzo unico di materiali autologhi, osso autologo, fattori di crescita e staminali autologhe.
Il paziente viene preparato con i campi magnetici che trasferiscono un’informazione riparativa, sottoponendolo ad induzione magnetoelettrica con programma di rigenerazione tessutale per circa 20 min. subito prima dell’intervento. Questa prima fase fondamentale permette di attivare le cascate morfogenetiche riparative prima che si crei la lesione chirurgica. Amplificando il sensing ed il signaling tessutale si trasferisce l’informazione spazio-temporalizzata di riparazione (cellula e tessuto informato).
In sala operatoria, il paziente viene preparato con un’agocannula in vena per il prelievo di sangue che poi andrà nel separatore di fase per la preparazione del bCGF. La stessa agocannula servirà per la gestione di eventuali complicanze in fase operatoria.
Il bCGF è costituito da una serie di fasi che si separano in relazione al peso molecolare dei componenti liquidi e corpuscolati. Avremo quindi una prima fase costituita dal siero, una seconda costituita dal “ fibrin buffy coat” che è un condensato fibrinico con una polimerizzazione
densa tanto che può essere trattato e posizionato come fase semi-solida, creando uno scaffold naturale 3D su cui aderiscono le staminali e si differenziano. Lo scaffold 3D è il presupposto per creare una comunicazione chimico-fisica fra i margini del tessuto leso. Le proteine filamentose
sono dotate di caratteristiche biofisiche sorprendenti e fra queste la loro piezoelettricità dovuta ad un forte momento dipolare. Poiché il mezzo circostante, cioè la matrice possiede una costante dielettrica bassa le reazioni chimiche risultano facilitate. Per la loro struttura le fibrille collagene si comportano come semiconduttori, per cui il flusso di elettroni sulla
loro superficie è a senso unico, come nei diodi. Perciò a seconda della disposizione relativa tra fibrille e cellule, si potrebbero differenziare delle fibrille afferenti ed efferenti. Questo concetto vale per tutte le proteine fibrillari ed in particolare per il collageno, secondo scaffold riparativo. Il collagene, come ogni struttura peptidica è capace di risonanza. Ciò dà luogo a -elettroni delocalizzati, il che fa accelerare l’accoppiamento coerente di fotoni e il trasporto vettoriale di impulsi d’energia, vale a dire d’informazione.(4) ( F. Crescentini 2011 ).
Nella 3° fase troviamo i fattori di crescita piastrinici e le staminali CD34+ che sono fortemente angiogenetiche. Nella quarta fase troviamo il “red buffy coat” costituito da piastrine integre e dalle altre parti corpuscolare del sangue.

Dobbiamo ricordare che le piastrine dal punto di vista biofisico sono i migliori superconduttori1 che esistano e si comportano come ripetitori di energia bioelettrica.
Le condizioni biologiche indispensabili per la funzionalizzazione dei concentrati piastrinici sono:
Dopo la centrifugazione le piastrine devono essere integre.
Corretto dosaggio fra velocità di centrifugazione e tempo di centrifugazione.
La tensione parziale di ossigeno deve rimanere entro limiti compatibili.
Il ciclo dell’ossigeno piastrinico deve essere conservato.
1 Superconduttività: Assenza di perdite a 3 valori critici:
- temperatura,
- densità di corrente
- campo magnetico
a tensione parziale di ossigeno dei tessuti del sito ricevente deve essere mantenuto a livelli compatibili.
Il sito ricevente deve rimanere sterile.
Il sito ricevente non deve modificare il Ph.
Una volta posizionato il concentrato non deve essere più rimosso.
L’aggregazione e l’attivazione delle piastrine dipende dalle traiettorie impresse, dal meccanismo di collisione, dal tempo di collisione, dalla caratteristica della collisione, dalla sua frequenza e dall’area di contatto fra le pareti delle piastrine. Questo ne induce l’aggregazione e l’attivazione anche in assenza di danno vascolare e quindi dall’attività delle proteine delle membrane endoteliali. (8) Queste problematiche sono state in buona parte risolte dalla VLAD ( Blood’s Fases Separator) che peraltro nella sua forma più evoluta tiene conto e viene programmato anche in relazioni alle condizioni generali del paziente e quindi delle sue patologie sia ematologiche (anemie, eccessi o difetti di concentrazione ecc.) che altre ( connettiviti, errori metabolici, tumori, ecc). I mezzi biotecnologici sono rappresentati dal bCGF, Blood’s Concentrated Growth Factors, ottenuti attraverso un separatore di fase ( VLAD – Pressing , SMR )
I mezzi fisici utilizzati sono: i campi magnetici ( Seqex MED), i laser a ottica non lineare 532nm ( Lasering srl ).
Le motivazioni che ci hanno indotto ad utilizzare i succitati mezzi fisici sono i seguenti:
1- Necessità di abbattere il biofilm batterico-fungino in maniera irreversibile.
2- Necessità di stimolare l’angiogenesi ridotta dai difosfonati e non ripristinabile farmacologicamente.
3- Innescare un processo riparativo molto veloce nonostante la necrosi ossea autogenerante.
Si devono quindi innescare le patways rigenerative chiudendo la porta ai batteri e ai funghi nel minor tempo possibile per evitare che si riformi il biofilm.
Con i mezzi di cui disponiamo abbiamo impostato un protocollo multifattoriale che ci permette un’accelerazione di tutte e cinque le fasi riparative ossee e di quelle mucose secondo il seguente schema:
Accelerazione programmata delle fasi riparative.
Fase 1 coaugulativa: campi magnetici polarizzazione parti corpuscolate del sangue accelerazione della coagulazione.
Fase 2 macrofagica: Laser, campi magnetici. Riduzione dell’infiammazione relativamente ad una miglior qualità dell’incisione, alla qualità del debridment osseo, alla microfoto-
ablazione, alla fotobiomodulazione Laser, e alla modulazione delle interleuchine campi magnetici. All’effetto antibatterico Laser-magnetico, Laser- campi magnetici.
Fase 3 di matrice proteica: Folding proteico +GF+supporto alle staminali, bCGF, stimolazione della mitosi e dell’espressione genica dei morfogeni, bCGF- campi magnetici.
Fase 4 cascate osteomorfogenetiche: Effetto osteomorfogenetico dei campi magnetici,
Fase 5 di rimodellazione: Modulazione dell’osteoclastogenesi e quindi del rimodellamento con campi magnetici .
Finalità dello studio
Utilizzare la chirurgia microscopica laser-magneto- assistita per evitare nella terapia chirurgica delle BRONj procedure invalidanti e ottenere una rapidissima riparazione tessutale senza/minima perdita dimensionale ossea. Evitare le complicanze post operatorie e i disagi legati al dolore all’edema e all’infiammazione oltre che alle infezioni specie se farmaco-resistenti stimolando i tessuti a rigenerare rapidamente, evitando così infezioni secondarie e ritardi riparativi che possano modificare la guarigione clinica.
Caso clinico esplicativo
Paziente donna di 84 anni in terapia con difosfonati (Fosamax e altri) da 10 anni per pregresso tumore del seno. Focolaio diagnosticato molto tardivamente solo a causa di una forte alitosi.

a) Rx iniziale

b) Immediato post chirurgico

c) Riparazione a 10 giorni delle mucose – nessuna cicatrice, nessun vallo in sedazione cosciente.
E’ stata praticata terapia antibiotica e antimicotica prima e dopo l’intervento. E’ ancora più interessante dal punto di vista biologico notare come si possa guidare l’osteomorfogenesi (9-10) con le radiazioni ultradeboli complesse e con i laser non lineari a luce verde (11) oltre che con uno scaffold autologo.

d) Riparazione ossea a 45 giorni

e) Notare la quantità di osso rigenerato e come i vettori di calcificazione seguano esattamente la direzione dei patch di bCGF posizionati (a) nonché lo sviluppo osseo verticale (b)

f) Visione del focolaio prima del trattamento chirurgico e dopo 45 Immagini a confronto
Conclusioni
Il lavoro tende a dimostrare che è possibile utilizzare un protocollo chirurgico multifattoriale in chirurgia microscopica servendosi di mezzi fisici e biotecnologici, con la finalità di ottenere la guarigione clinica dell’osteonecrosi da difosfonato, senza menomazioni chirurgiche e senza o con minime perdite della dimensione ossea evitando, al paziente tutto o quasi il corredo sintomatologico post-chirurgico. Ciò apre la strada ad una nuova procedura chirurgica nelle osteonecrosi in generale ed in particolare nella BRONj.
Considerazioni
E’ interessante notare come attraverso tecnologie evolute, si sia ottenuta una neo-osteomorfogenesi 3D con un callo osseo che nella sua strutturazione viene guidato dallo scaffold fibrinico riproducendone i vettori biofisici su cui avviene la calcificazione.
La paziente non ha avuto sanguinamento, febbre, dolore, parestesie e nemmeno edema nel post-chirurgico. E’ stata trattata
1-M. CORIGLIANO1, L. SACCO, A. CIPOLLINA, F. CRESCENTINI, and E. BALDONI Concentrated Growth Factors (CGFs) in the Restorative Tissue Techniques. J Dent Res 89 ( Spec Iss B ) : 4691,
2010
2- M. CORIGLIANO, A. CIPOLLINA, F. CRESCENTINI1, L. SACCO, and E. BALDONI2 The Surgical Multi-factorial Protocol for Bone and Soft Tissue Regeneration. J Dent Res 89 ( Spec Iss B ) :
3248, 2010
3- Cipollina A, Corigliano M, Crescentini F. BISPHOSPHONATE-RELATED OSTEONECROSIS OF JAW: A LOW SURGICAL IMPACT THROUGH NON-LINEAR LBO LASER AND ULTRAWEAK MULTIFREQUENCY COMPLEX MAGNETIC FIELDS 2011 Atti del Congresso WFLD-Int J Laser In Medical Science
2011
4 – CRESCENTINI F., Le Basi Epistemologiche del Sistema Informazionale Biologico Ed. Simple 2011- ISBN: 978-88-6259-330-4
5- Miller MB, Bassler BL. Quorum sensing in
Mody NA, King MR. Department of Chemical Engineering, University of Rochester, Rochester, New York, USA. Biophys J. 2008 Sep;95(5):2539-
- Epub 2008 May 30
9- Osteoneomorphogenesis biostimulated by
Combined Magnetic Field
- CORIGLIANO , S. ROSSI , F. CRESCENTINI , A. GIOVANNETTI , S. DI CARLO. J Dent Res 87 ( Special ISS B) : 2519,2008
11- The Surgical Multi-factorial Protocol for Bone and Soft Tissue Regeneration. M. CORIGLIANO1,A. CIPOLLINA1, F. CRESCENTINI1, L. SACCO1, and E. BALDONI2 J Dent Res 89 ( Spec Iss B ) :3248, 2010
ria. Department of Molecular Biology, Princeton University, Princeton, New Jersey 08544- 1014, USA. mmiller@molbio.princeton.edu. Annu Rev Microbiol. 2001;55:165-99.
6- Schneckenburger H, Hendinger A, Sailer R, Strauss WS, Schmitt M. Laser-assisted optoporation of single cells. Institut für Angewandte Forschung, Fachhochschule Aalen, 73428 Aalen, Germany. herbert.schneckenburger@fh-aalen.de
J Biomed Opt. 2002 Jul;7(3):410-6.
8-
7- . .Binhi VN, Alipov YD, Belyaev IY. Effect of static magnetic field on E. coli cells and individual rotations of ion-protein complexes.General Physics Institute Russian Academy of Sciences, Moscow,